Artritis psoriásica
Actualmente se sabe que la AP suele conducir a un deterioro de la función y la calidad de vida. Sin embargo, el mejor conocimiento de los mecanismos de la enfermedad ha catalizado el rápido desarrollo de terapias eficaces.Autor: Christopher T. Ritchlin, Robert A. Colbert, Dafna D. Gladman. Psoriatic Arthritis. N Engl J Med 2017;376:957-70.
| Resumen: La psoriasis es una enfermedad común de la piel que se asocia con múltiples condiciones coexistentes, siendo la más prevalente, la artritis psoriásica (AP), que se desarrolla hasta en un 30% de los pacientes con psoriasis y se caracteriza por diversas manifestaciones clínicas. A menudo, ésto resulta en un retraso en el diagnóstico y tratamiento. Los informes iniciales enfatizaron un curso benigno en la mayoría de los pacientes, pero actualmente se sabe que la AP suele conducir a un deterioro de la función y la calidad de vida. Sin embargo, el mejor conocimiento de los mecanismos de la enfermedad ha catalizado el rápido desarrollo de terapias eficaces. |
♦ Artritis psoriásica y espondiloartrosis
La descripción clásica de las características clínicas de la AP se publicó en 1973. Sin embargo, los restos esqueléticos desenterrados en 1983 en un monasterio bizantino del desierto de Judea, que datan del siglo V d.C, mostró imágenes visuales y radiográficas características coincidentes con las de la enfermedad psoriásica ósea y articular. La AP comparte características genéticas y clínicas con otras formas de espondiloartritis y se la clasifica junto a estos trastornos. Los criterios diagnósticos para la AP no han sido validados pero los Classification Criteria for Psoriatic Arthritis (criterios CASPAR) publicados en 2006 expresan una definición de la AP con el fin de enrolar a los pacientes en ensayos clínicos y así proporcionar una orientación a los médicos.
| Criterios de clasificación de la artritis psoriásica (CASPAR)* | ||
| Criterio | Explicación | Puntos |
| ► Evidencia de psoriasis Psoriasis actual Historia de psoriasis Historia familiar de psoriasis | Enfermedad psoriásica actual de la piel o del cuero cabelludo según lo juzga un dermatólogo o reumatólogo. Historia de psoriasis según el paciente o el médico de cabecera, dermatólogo o reumatólogo. Historia de psoriasis en un paciente de primer o segundo grado, según el paciente. |
2
1
1
|
| ► Distrofia psoriásica ungular | Distrofia típica de uña psoriásica (por ej., onicólisis, poceado o hiperqueratosis) según observación durante el examen físico actual. |
1
|
| ► Test (-) de factor reumatoideo | Basado en el rango de referencia en el laboratorio local; cualquier método de prueba excepto látex con preferencia por ELISA o nefelometría. |
1
|
| ► Dactilitis Dactilitis actual Historia de dactilitis | Inflamación de un dígito entero según la observación en el examen físico actual Según el dermatólogo |
1
1
|
| ► Signos radiográficos de formación ósea nueva yuxtaarticular | Osificación mal definida cerca de los márgenes articulares (excluyendo la formación de osteofitos) en radiografías simples de mano o pie |
1
|
| *Se considera que la AP está presente en pacientes con enfermedad musculoesquelética inflamatoria (implica la articulación, la columna vertebral o la entesis) cuya calificación en los 5 criterios enumerados en la tabla suma al menos 3 puntos. El criterio "evidencia de psoriasis" puede explicar 1 o 2 puntos. Los criterios tienen una especificidad del 98,7% y una sensibilidad del 91,4%. ELISA: análisis inmunoenzimático | ||
♦ Epidemiología y carga de la enfermedad
En la población de EE. UU., la prevalencia de AP oscila entre 6 y 25 casos/10.000 personas, dependiendo de la definición del caso. Hasta ahora se creía que la AP era rara pero estudios recientes basados en los criterios CASPAR indican que ocurre hasta en un 30% de los pacientes con psoriasis. Estos datos sugieren que su prevalencia es de 30 y 100 casos/10.000, suponiendo que el 3% de la población de EE.UU. tiene psoriasis. Alrededor del 15% de los pacientes con psoriasis que son seguidos por dermatólogos tiene AP no diagnosticada.
En un estudio prospectivo de pacientes con psoriasis, la incidencia de AP fue de 2 a 3%. La manifestación de la psoriasis precede a la de la artritis en el término de un promedio de 10 años, aunque en el 15% de los casos, la artritis y la psoriasis se presentan en forma simultánea, o la AP precede a la enfermedad de la piel. La AP es poco común en los asiáticos y las personas de raza negra, y la proporción entre hombres y mujeres es de 1: 1, pudiendo comenzar en la infancia. Hay 2 subtipos clínicos que no se excluyen mutuamente. La AP oligoarticular (caracterizada por la afectación de ≤4 articulaciones) tiene un pico de inicio a los 1 a 2 años de edad y se produce predominantemente en niñas.
Esta forma se asocia a una prueba positiva para anticuerpos antinucleares y uveítis crónica, y a menudo se caracteriza por dactilitis (hinchazón difusa de un dedo de la mano o del pie). El segundo subtipo (caracterizado por la afectación de cualquier número de articulaciones) se desarrolla entre los 6 y los 12 años de edad y se asocia con HLAB27; generalmente, los anticuerpos antinucleares están ausentes. Esta forma tiene una proporción de sexos 1: 1, con dactilitis, entesitis (inflamación en el tendón, ligamento o inserciones de la cápsula articular), poceado ungular, onicólisis y afectación axial, con mayor frecuencia que en el primer subtipo.
De acuerdo con el sistema de clasificación de la International League of Associations for Rheumatology, la AP es distinta de otras formas de artritis idiopática juvenil y se define por la coexistencia de AP en ausencia de las características de las otras formas de artritis idiopática juvenil. Un niño con artritis que no tiene psoriasis pero tiene ≥2 características de AP, como dactilitis, poceado ungular, onicólisis o historia familiar de psoriasis (pariente de primer grado), cumple los criterios para el diagnóstico de AP.
Las cargas psicológicas y funcionales de la enfermedad son considerables y de una magnitud similar a las de la espondiloartritis axial y la artritis reumatoidea. Un estudio mostró que la AP se asoció significativamente con mayores tasas de ausentismo laboral y tasas bajas de productividad, y que estos hallazgos se correlacionaron con las mediciones de la actividad de la enfermedad y el rendimiento físico. Las tasas de mortalidad entre los pacientes con AP han caído y son similares a las de la población general, aunque algunos centros informan un aumento por enfermedad cardiovascular.
♦ Manifestaciones clínicas
Moll y Wright describieron 5 subtipos clínicos de AP que destacan la heterogeneidad de la enfermedad. El subtipo oligoarticular afecta a ≤4 articulaciones y normalmente se presenta con una distribución asimétrica. El subtipo poliarticular afecta a ≥5 articulaciones; el compromiso puede ser simétrico y se asemeja a la artritis reumatoidea.
El subtipo distal, que afecta las articulaciones interfalángicas distales de las manos, pies o a ambas, suele ocurrir con otros subtipos, y aparece solo en el 5% de los pacientes. La artritis mutilarte, un subtipo de artritis deformante y destructivo que implica una marcada resorción ósea u osteólisis y se caracteriza por el telescopado y plegado de los dedos. El subtipo axial o espondiloartritisinvolucra principalmente a la columna vertebral y las articulaciones sacroilíacas. Estos patrones pueden cambiar con el tiempo.
La entesitis se observa en el 30 al 50% de los pacientes y más comúnmente afecta la fascia plantar y el tendón de Aquiles, pero puede causar dolor alrededor en la rótula, la cresta ilíaca, los epicóndilos y las inserciones del supraespinoso. En el 40 al 50% de los pacientes se informa dactilitis, la cual es más prevalente en el tercer y cuarto dedo de los pies, pero también puede comprometer los dedos de la mano. La dactilitis puede ser aguda (inflamación, enrojecimiento cutáneo y dolor) o crónica (inflamación sin inflamación). La dactilitis a menudo se asocia con la enfermedad grave caracterizada por poliartritis, erosión ósea y formación de hueso nuevo.
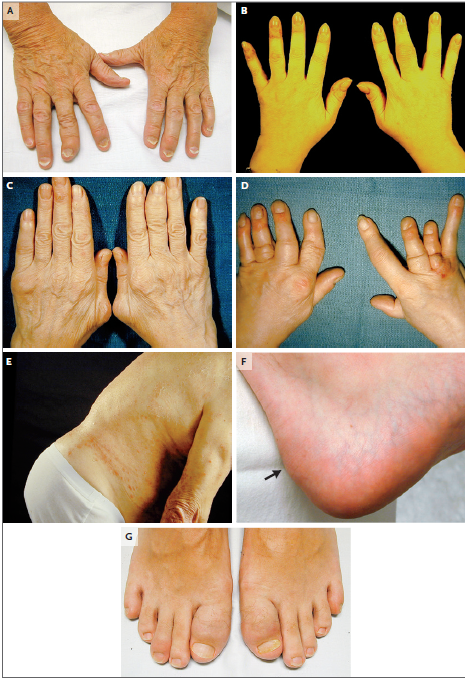
(Fig. 1) Características clínicas de la AP. Panel A: subtipo distal de la AP, con onicólisis adyacente. Panel B: subtipo oligoarticular. Panel C: subtipo poliarticular. Panel D: artritis mutilante, con telescopado digital y compromiso asimétrico y diferencial de los dígitos adyacentes. Panel E: subtipo de espondilitis. Panel F: entesitis del tendón de Aquiles (flecha). Panel G: dactilitis de los dedos de los pies.
El diagnóstico de AP se basa en el reconocimiento de las características clínicas y de las imágenes, ya que no hay biomarcadores específicos. Es posible que participen al menos 5 dominios: psoriasis, enfermedad articular periférica enfermedad axial, entesitis y dactilitis. Los pacientes deben ser evaluados cuidadosamente para detectar estos dominios, teniendo en cuenta que en un individuo pueden estar presentes varios de ellos. A menudo, las historias personal y familiar de la psoriasis son positivas.
La artritis inflamatoria, la entesitis, la dactilitis y la distribución de las articulaciones afectadas proporcionan pistas diagnósticas importantes, al igual que ciertas características como la presencia de enfermedad inflamatoria intestinal y uveítis. Es importante buscar lesiones cutáneas psoriásicas, particularmente en la ingle, la zona umbilical, el cuero cabelludo, las orejas y las nalgas (por ej., pliegue interglúteo). Las lesiones de las uñas, incluyendo pozos y onicólisis así como la presencia de enfermedad espinal apoyan el diagnóstico.
Es importante que los dermatólogos y los médicos de atención primaria que atienden a los pacientes con psoriasis identifiquen precozmente la AP. Los pacientes con psoriasis deben ser interrogados acerca del dolor en las articulaciones, rigidez matinal y signos de dedos en "salchicha" (dactilitis). Los cuestionarios de cribado para los dermatólogos y médicos de atención primaria ofrecen una elevada sensibilidad para detectar problemas musculoesqueléticos, pero son de una especificidad moderada para la AP.
♦ Diagnóstico diferencial
El diagnóstico diferencial es necesario para diferenciar la AP de la artritis reumatoidea, la artrosis, la gota, la seudogota, el lupus eritematoso sistémico y otras formas de espondiloartritis.
| Diferenciación entre varias formas de artritis.* | ||||
Variable
|
Artritis psoriásica
|
Artritis reumatoidea
|
Gota
|
Artrosis
|
Distribución articular inicial
|
Asintomática
|
Simétrica
|
Asimétrica
|
Asimétrica
|
Nº articulaciones afectadas
|
Oligoarticular
|
Poliarticular
|
Poli u oligoarticular
|
Mono u oligoarticular
|
Sitios de amanos y pies afectados
|
DIstal
|
Proximal
|
Distal
|
DIstal
|
Áreas afectadas
|
Todas las articulaciones de un dedo
|
La misma articulación en todos los dedos
|
Usualmente monoarticular
|
La misma articulación en todos los dedos
|
Dolor (kg en el dolómetro
|
7
|
4
|
No evaluado
|
No evaluado
|
Decoloración púrpura
|
Si
|
No
|
Sí
|
No
|
Compromiso espinal
|
Común
|
Infrecuente
|
Ausente
|
No inflamatoria
|
Sacroileítis
|
Común
|
Ausente
|
Ausente
|
Ausente
|
La artritis reumatoide se caracteriza por la afectación proximal y simétrica de las articulaciones de las manos y los pies, respetando las articulaciones interfalángicas distales, mientras que en más del 50% de los pacientes con AP las articulaciones distales están afectadas. El compromiso tiende a caracterizarse por una distribución en "rayo", con todas las articulaciones del mismo dedo afectadas e indemnidad de los otros dígitos.
Esto se nota tanto clínicamente como en las radiografías. Al comienzo, la AP tiende a ser oligoarticular y menos simétrica que la artritis reumatoidea, pero con el tiempo puede llegar a ser poliarticular y simétrica. Las articulaciones afectadas son menos en la AP que en la artritis reumatoidea y puede haber una decoloración purpúrea. El compromiso de la columna vertebral (articulaciones o lumbares o sacroilíacas, torácicas o cervicales) ocurre en más del 40% de los pacientes con AP pero es rara en los pacientes con artritis reumatoidea.
La monoartritis psoriásica, que particularmente afecta los dedos de los pies, o dactilitis, puede ser diagnosticada como gota o seudogota. La uricemia puede ser elevada en los pacientes con AP así como en aquellos con gota, haciendo difícil el diagnóstico diferencial, en particular si no se hallan cristales en el análisis del líquido sinovial o su análisis no puede realizarse. La afectación de la articulación distal, que es característica de la AP. también se observa en la artrosis.
En la AP, la palpación de las articulaciones revela hinchazón leve debido a la inflamación, mientras que en la artrosis la hinchazón surge por un osteofito óseo y es sólida. Por otra parte, la participación de las articulaciones interfalángicas distales y la enfermedad de las uñas (poceado u onicólisis) ocurren con frecuencia en la AP pero no en la artrosis.
La espondilitis anquilosante típicamente tiene un comienzo tardío, en la segunda década de vida o al comienzo de la tercera, mientras que la espondiloartritis psoriásica es más probable que se desarrolle en la cuarta década de vida. La espondiloartritis psoriásica puede ser menos grave que la espondilitis anquilosante, con menos dolor y poca frecuencia de anquilosis sacroilíaca; Una distribución asimétrica de sindesmofitos (crecimiento óseo originado en un ligamento de la columna vertebral) es más frecuente en la AP.
Puede ser difícil distinguir entre la AP y la artritis reactiva. Ambas condiciones pueden estar asociadas a lesiones articulares y cutáneas, siendo éstas últimas difíciles de atribuir patológicamente una de la otra. Las lesiones psoriasiformes del lupus cutáneo subagudo pueden simular la psoriasis vulgar, pero los pacientes con lupus cutáneo no muestran las otras características definitorias de la AP.
♦ Hallazgos en los análisis de laboratorio e imágenes
Las pruebas para el factor reumatoideo, el péptido anticíclico citrulinado, o ambos, son negativos en el 95% de los pacientes con AP. Para diferenciar el psoriasis de la artritis reumatoidea cuando un test es positivo hay que basarse en las características clínicas y de las imágenes. Casi el 25% de los pacientes con AP son positivos para HLA-B27.
El aumento del nivel de proteína C reactiva sérica, de la velocidad de eritrosedimentación o de ambas ocurre solo en el 40% de los pacientes. La presencia de destrucción ósea y cartílaginosa con formación de hueso nuevo patológico es uno de los aspectos más distintivos de la AP.
 (Figura 2) ♦ Características radiográficas de la AP
(Figura 2) ♦ Características radiográficas de la AP| A: artritis mutilante, con deformidades “lápiz en copa” (flecha) y marcada resorción ósea (osteólisis) en las falanges de la mano derecha. B: La radiografía muestra resorción de las articulaciones, anquilosis y erosión en un solo rayo. C: entesofitos en la fascia plantar e inserciones del tendón de Aquiles. D: sindesmofitos en la columna cervical, con anquilosis de las articulaciones facetarías (flecha). E: sacroileítis bilateral grado 3. F: sindesmofito paramarginal en 4ª y 5ª vértebras lumbares. G: edema de la médula ósea en la 2ª y 3ª vértebras lumbares en un paciente con psoriasis grave y un nuevo inicio de dolor de espalda. H: la ecografía en escala de grises de alta frecuencia (15 MHz) muestra sinovitis de la articulación metacarpofalángica. Hay distensión de la cápsula articular (flechas). Las señales confluentes rojas (recuadro en la parte inferior de la imagen) con ecoDoppler de potencia indican hiperemia sinovial. MC: cabeza metacarpiana. PP: falange proximal. La ecografía de alta frecuencia (15 MHz) I: La ecografía de alta frecuencia muestra entesitis. Las señales confluentes rojas del ecoDoppler de potencia representan hiperemia en el tendón, cerca de su inserción en el calcáneo. Normalmente, los tendones están poco vascularizados. |
Las radiografías de las articulaciones periféricas suelen mostrar pérdida ósea con erosiones excéntricas y estrechamiento del espacio articular, así como formación ósea nueva caracterizada por periostitis, anquilosis ósea y entesofitos (proyecciones óseas anormales en la unión de un tendón o ligamento).
En el esqueleto axial, los cambios asociados a la AP incluyen la sacroileítis unilateral y voluminosos sindesmófitos paramarginales y verticales. (En contraste, en la espondilitis anquilosante, la afectación sacroilíaca suele caracterizarse por sindesmofitos bilaterales y paramarginales, poco comunes.)
La resonancia magnética puede revelar erosiones focales, sinovitis y edema de la médula ósea en la región periférica y estructuras axiales, particularmente en la entesis. El edema de la médula ósea se observa mejor con la técnica de las secuencias de recuperación de la inversión de tau corto con supresión grasa, en la T2 ponderada (STIR). La ecografía Doppler de potencia puede identificar la sinovitis, el aumento del flujo, la tenosinovitis, los entesofitos y la enfermedad erosiva precoz.
♦ Resultados
La AP es una forma grave de artritis. Las deformaciones y los daños articulares se desarrollan en gran número de pacientes. En el 47% de los pacientes se observan erosiones óseas en los primeros 2 años, a pesar de que en más de la mitad de los pacientes se utilizan los medicamentos tradicionales modificadores de la enfermedad.
Por otra parte, la enfermedad grave al inicio de la enfermedad y la elevación del nivel de la proteína C reactiva son factores de riesgo de progresión radiográfica. La remisión espontánea de la AP es extremadamente rara. En un ensayo de observación en el que participaron pacientes tratados con el factor de necrosis antitumoral (TNF), la tasa de remisión parcial fue del 23%. Sin embargo, cuando los agentes son interrumpidos las tasas de recaída son elevadas.
♦ Condiciones coexistentes
La AP se asocia con obesidad, diabetes tipo 2, hipertensión, síndrome metabólico, hígado graso y mayor riesgo cardiovascular. La uveítis que afecta los polos posteriores del ojo ocurre en el 8% de los pacientes con AP. En ellos, la prevalencia de la enfermedad de Crohn y la colitis subclínica es mayor.
♦ Causas y características fisioipatológicas
La AP es una enfermedad hereditaria altamente poligénica. La razón de riesgo de recurrencia (definida como el riesgo de manifestación de la enfermedad en hermanos vs. riesgo en la población general) es mayor que, lo cual es sustancialmente superior al riesgo de recurrencia de la psoriasis o la artritis reumatoidea.
En contraste con esta última, que se asocia con los alelos del complejo de histocompatibilidad mayor (MHC) de clase II, la psoriasis y la AP se asocian con los alelos del MHC de clase I Más notable es que HLA-C*06 es un factor de riesgo importante para la psoriasis pero no para la AP. En ésta se han observado las frecuencias de HLA-B*08; B*27; B*38 y B*39 con subtipos específicos de los alelos vinculados a los subfenotipos, incluyendo la enfermedad axial simétrica o asimétrica, la entesitis, la dactilitis y la sinovitis.
Las exploraciones de asociación de todo el genoma han demostrado ciertos polimorfismos en el gen que codifica al receptor de interleucina-23 (IL23R), junto con variantes en la expresión génica del factor nuclear κB (NF-κB) (TNIP1) y la señalización (TNFAIP3), y la expresión del TNF asociada a la AP. Un polimorfismo en el cromosoma 5q31, rs715285 traza un mapa en una región intergénica flanqueada por los genes CSF2 y P4HA2. Los estudios de asociación han Identificado alelos de riesgo adicionales en pacientes con psoriasis y AP, incluyendo las IL12A, IL12B, IL23R y los genes que regulan el NF-κB.
Existen varios factores de riesgo ambiental ara la AP, entre los que se encuentran la obesidad; la psoriasis grave; la afectación del cuero cabelludo y los genitales y, la psoriasis inversa (tipo intertrigo); además, la enfermedad de las uñas y el trauma o las lesiones profundas en sitios que sufren traumatismos (fenómeno de Koebner).
Se ha demostrado consistentemente que las células T son importantes en la psoriasis y la AP. Las células T CD8+ tienen un papel central en la patogénesis de la enfermedad, que es apoyado por la asociación con los alelos HLA de clase I, la expansión de las células T CD8+ oligoclonales y la asociación de la AP con la enfermedad por el VIH.
Las células de tipo 17, que incluyen las CD4+ tipo 17 helper T (Th17) y los linfocitos innatos de tipo 3 (células productoras de IL-17A e IL22) junto con los linfocitos CD4+CD8+, se incrementan en el líquido sinovial psoriásico comparado con el líquido sinovial reumatoideo.
Estudios recientes destacan la importancia de IL-23-IL-17 y las vías TNF en la patogénesis de la psoriasis, la AP y las espondiloartropatías axiales. En la psoriasis, la expresión de interferón-α por las células dendríticas plasmacitoides activa las células dendríticas dérmicas que activan la diferenciación de las células T de tipo 1 (Th1) helper y las células Th17 en los ganglios linfáticos. Estos linfocitos retornan a la dermis y orquestan un complejo inflamatorio inmemediado. Además de los factores genéticos, los factores de riesgo ambientales o ambos son propensos a desencadenar la artritis inflamatoria.
En un modelo de enfermedad alternativo se propone que la entesis es el sitio inicial de la enfermedad musculoesquelética. En apoyo de este punto de vista, la entesitis, la sinovitis y la alteración de la remodelación ósea en un modelo murino en el que se administró IL-23 condujo a una artritis inflamatoria centrada en la entesitis, que era similar a la espondiloartritis, con erosión ósea y formación de hueso nuevo. La inflamación estaba vinculada a una población nueva de linfocitos innatos residentes en la entesis, productores de IL-17.
La inflamación y la erosión ósea fueron mediadas por el TNF y la IL-17. Otro modelo murino demostró que la sobreexpresión de IL-23 también puede conducir a una artritis inflamatoria de fenotipo erosivo, que puede reflejar diferencias en la dosis o el momento de la administración de la IL-23, la heterogeneidad bacteriana o las diferencias en las cepas de ratón.
Posteriormente, se han obtenido informes de varios modelos murinos de espondiloartrosis con entesitis, lesiones cutáneas psoriasiformes y artritis que utilizaron IL-23 Las infecciones microbianas son causas conocidas de formas de espondiloartritis y existen informes de que en los apacientes con AP hay mayor frecuencia de inflamación intestinal subclínica y disbiosis (disminución de la diversidad microbiana), en comparación con los controles sanos, lo que apoya la posible participación Intestinal en la patogénesis de la AP.
En los pacientes con AP, los tejidos sinoviales tienen un parecido más cercano a la sinovial de los pacientes con espondiloartritis que a la sinovial de aquellos con artritis reumatoidea, con mayor vascularización y afluencia de neutrófilos y ausencia de anticuerpos anti péptidos citrulinados. En comparación con el tejido reumatoideo sinovial, el tejido sinovial psoriásico tiene menor número de linfocitos T infiltrantes y células plasmáticas, pero la expresión de TNF y de IL-1, IL-6 e IL-18 es similar en las dos enfermedades.
En la AP, la afectación ósea es heterogénea, tanto entre los pacientes como en cada paciente individual. La afectación espinal puede ser similar a la de la espondilitis anquilosante y las características destructivas de las articulaciones periféricas pueden ser como las de la artritis reumatoidea. En los sitios de inflamación de los tejidos blandos típicamente se produce la formación de hueso nuevo patológico, incluyendo anquilosis articular y sindesmofitos.
En la sinovial psoriásica hay una marcada regulación hacia arriba del receptor activador de NF-κB (RANK) (RANKL) y una expresión baja de su antagonista, la osteoprotegerina, como ha sido detectado en el recubrimiento sinovial adyacente. La citocina RANKL se une a RANK en la superficie de los precursores de los osteoclastos derivados de los monocitos CD14+ circulantes. Esta interacción ligando-receptor desencadena la proliferación de los precursores de los osteoclastos y su diferenciación en osteoclastos multinucleados, responsables de la resorción ósea.
Por otra parte, un estudio ha demostrado que los precursores de los osteoclastos derivados de los monocitos CD14+ circulantes están muy elevados en la sangre periférica de los pacientes con AP, en comparación con los controles sanos, y que el tratamiento con agentes anti-TNF reduce significativamente el nivel de precursores circulantes, un hallazgo que apoya un efecto central de TNF en la generación de la formación de precursores. Las moléculas y las vías asociadas a la formación ósea patológica son la IL-17A, la proteína morfogenética ósea, el factor de crecimiento transformandor β, la prostaglandina E2 y las moléculas de la vía de señalización Wnt, aunque su papel en la AP se desconoce.
♦ Medición de los resultados del tratamiento de la artritis psoriásica
En los pacientes con AP es importante evaluar cada uno de los problemas de los dominios musculoesqueléticos, además de la gravedad y la extensión de la psoriasis. Las evaluaciones deben incluir: el examen de 68 articulaciones para detectar el dolor y de 66 articulaciones para detectar la inflamación; la amplitud del movimiento espinal, la entesitis, evaluada utilizando índices de entesitis como el Leeds Enthesitis Index (evaluación de 6 entesis), o el Spondylarthritis Research Consortium Canadá (SPARCC) Enthesitis Index y, la dactilitis, evaluada mediante el recuento de los dedos con dactilitis o usando el Leeds Dactylitis Index.
La psoriasis debe evaluarse teniendo en cuenta las áreas de la superficie corporal afectadas, mediante el Psoriasis Área and Severity Index (PASI); se deben examinar las uñas para buscar onicólisis o poceado.
En ensayos clínicos, las medidas de los resultados adaptadas de los instrumentos utilizados para evaluar los resultados de la artritis reumatoide incluyen las tasas de respuesta al American College of Rheumatology (ACR) 20, ACR 50, y el ACR 70 (lo que indica una reducción del número de articulaciones tanto hinchadas como dolorosas de al menos 20%, 50% y 70%, respectivamente, con mejoría en al menos 3 de las siguientes 5 mediciones adicionales: evaluación global hecha por el paciente y el médico y, la evaluación del dolor, la discapacidad, de un reactante de fase aguda) y mediante el Disease Activity Score (DAS), que se utiliza para evaluar la artritis periférica.
Recientemente se ha desarrollado una serie de mediciones combinadas específicas para la AP, incluyendo el uso del Psoriatic Arthritis Disease Activity Score, el Composite Psoriatic Disease Activity Index y, el instrumento GRACE (Group for Research and Assessment of Psoriasis and Psoriatic Arthritis [GRAPPA] Composite Exercise). Por otra parte, la baja actividad de enfermedad, definida por una mejoría clínica significativa en 5 de las 7 medidas de respuesta o dominios, es un instrumento validado para evaluar la respuesta de la AP al tratamiento.
♦ Tratamiento
El tratamiento de la AP es complicado debido a la heterogeneidad en la presentación de la enfermedad y a su curso, lo que a menudo resulta en el retardo del diagnóstico. Para abordar esta complejidad, es Importante identificar la actividad de la enfermedad en los dominios. El dominio con el nivel más elevado de actividad comanda las opciones terapéuticas, y es muy común que el paciente tenga comprometidos varios dominios. En la actualidad se han publicado recomendaciones terapéuticas basadas en la evidencia.
Para los pacientes con una presentación oligoarticular leve pueden ser efectivos los antiinflamatorios no esteroides combinados con inyecciones intraarticulares, cuando sea apropiado. Para los pacientes con síntomas más graves, como tratamiento inicial típicamente se prescriben fármacos antirreumáticos modificadores de la enfermedad (DMARD). Los autores se lamentan de la falta de datos de ensayos clínicos aleatorizados del tratamiento de la AP con DMARD. Un ensayo con metotrexato comparado con placebo no mostró un efecto terapéutico efectivo, aunque el estudio pudo haber sido insuficiente y la dosis de metotrexato fue menor a la prescrita habitualmente.
La leflunomida es efectiva para la AP periférica pero no para la psoriasis. Los datos muestran que los agentes anti-TNF (adalimumab, certolizumab, etanercept y golimumab) suprimen la inflamación cutánea y articular y retardan la progresión radiográfica. Estos agentes son eficaces para la entesitis, la dactilitis y también para la enfermedad axial, según los datos de ensayos con pacientes con diagnóstico de espondilitis anquilosante.
El uso del anticuerpo anti-p40 ustekinumab, dirigido contra la subunidad compartida de IL-12 e IL-23, es eficaz para el tratamiento de la psoriasis y la AP, aunque los resultados en la piel son más notables que en las articulaciones. El secukinumab y el brodalumab, agentes bloqueantes de la IL-17 y del receptor de la IL-17, respectivamente, son eficaces en la AP, con mejoría tanto en la piel como en las manifestaciones musculoesqueléticas. Sin embargo, los ensayos de brodalumab fueron suspendidos debido a problemas de seguridad que no fueron observados con el secukinumab.
El ixekizumab, otro bloqueante de la IL-17, demostró eficacia en ensayos de fase 3 de pacientes con AP y fue recientemente aprobado para el tratamiento de la psoriasis. La inhibición de la fosfodiesterasa 4 con apremilast ha sido aprobada para el tratamiento de la psoriasis y la AP. Las respuestas de la piel al tratamiento con apremilast son similares a las del metotrexato, pero las respuestas son algo inferiores a las observadas con los agentes biológicos. Finalmente, el abatacept, un bloqueante de la activación de las células T que apunta a las moléculas coestimuladoras CD80 y CD86, es moderadamente eficaz para la afectación articular de la AP pero no para la enfermedad de la piel.
Los agentes anti-TNF; el ustekimunab, los antagonistas de las IL-12-IL-23 y los anticuerpos monoclonales de IL-17, secukinumab y ixekizumab inhiben la progresión radiográfica en los pacientes con AP con compromiso de las articulaciones periféricas. El apremilast, el brodalumab y el secukinumab no son eficaces para el tratamiento de la artritis reumatoidea, mientras que el rituximab y el abatacept son altamente efectivos. En conjunto, estos hallazgos contrastantes con los de los ensayos clínicos sugieren que la artritis reumatoidea y la AP tienen diferentes mecanismos subyacentes.
Por el contrario, la fisiopatología de los trastornos cutáneos psoriásicos y de la enfermedad articular se superponen considerablemente. Sin embargo, en la AP, la ciclosporina y el metotrexato son más eficaces que la leflunomida. Estos hallazgos, junto con a la mayor respuesta a los agentes dirigidos a la IL-12-IL-23 en la piel, comparados con la respuesta en las articulaciones, subrayan los mecanismos divergentes de la inflamación en las placas psoriásicas y las articulaciones.
Aún no se dispone de un algoritmo de tratamiento específico para la AP juvenil que esté respaldado por evidencia de alto nivel. Las recomendaciones actuales siguen las guías para la artritis idiopática juvenil y se basan en las mediciones de la actividad de la enfermedad, incluyendo el número de articulaciones activas, los marcadores inflamatorios (velocidad de eritrosedimentación o nivel de proteína C reactiva) y las evaluaciones globales del médico y del paciente o de los padres.
Para planificar el tratamiento inicial y el escalonamiento de las dosis también se pueden utilizar indicadores de mal pronóstico como la afectación de ciertas articulaciones (por ej., cadera, muñeca, tobillo, columna cervical y sacroilíaca) y la presencia de signos de daño radiográfico.
Además de la farmacoterapia, se debe asesorar al paciente sobre la importancia de controlar la inflamación. La modificación del estilo de vida, incluyendo la cesación de fumar, el adelgazamiento, la protección de las articulaciones, la actividad física y el ejercicio, así como el manejo del estrés, también es vital para el tratamiento de la AP.
Resumen y comentario objetivo: Dra. Marta Papponetti